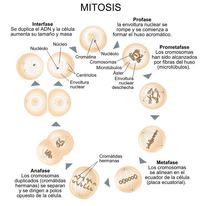
Diagrama que muestra el proceso de mitosis. Juliana Osorio. Click para ampliar.
Investigadores del Instituto de Investigación Biomédica de Bellvitge (IDIBELL) han identificado el mecanismo que permite a la proteína Zds1 regular un proceso clave en la mitosis, el proceso que ocurre en el núcleo de las células eucarióticas y que precede inmediatamente a la división celular, consistente en el reparto equitativo del material hereditario (ADN) característico.
El resultado de esta investigación se ha avanzado en la edición digital de la revista Journal of Cell Science y abre la puerta al desarrollo de terapias específicas y directas contra el cáncer.
Las células en todos los organismos crecen y se dividen en dos células hijas mediante una sucesión ordenada de eventos que se denomina “ciclo celular”. Las células tienen que completar cuatro procesos principales durante el ciclo celular: crecer (Fases de G1 y G2), duplicar el DNA (Fase S), segregar los cromosomas (Fase M, mitosis) y dividirse (citocinesis).
En la fase S, o replicación del DNA, se duplica el material genético y posteriormente durante la fase M, o mitosis, las células separan los cromosomas duplicados entre las dos células hijas. De esta forma se asegura la correcta herencia de la información genética de una generación de células a la siguiente.
El resultado de esta investigación se ha avanzado en la edición digital de la revista Journal of Cell Science y abre la puerta al desarrollo de terapias específicas y directas contra el cáncer.
Las células en todos los organismos crecen y se dividen en dos células hijas mediante una sucesión ordenada de eventos que se denomina “ciclo celular”. Las células tienen que completar cuatro procesos principales durante el ciclo celular: crecer (Fases de G1 y G2), duplicar el DNA (Fase S), segregar los cromosomas (Fase M, mitosis) y dividirse (citocinesis).
En la fase S, o replicación del DNA, se duplica el material genético y posteriormente durante la fase M, o mitosis, las células separan los cromosomas duplicados entre las dos células hijas. De esta forma se asegura la correcta herencia de la información genética de una generación de células a la siguiente.
Estabilidad cromosómica
La transmisión de la información genética (ADN) de padres a hijos (o lo que es equivalente, de unas células a otras) es una cuestión fundamental en la biología. La aneuploidia, es decir la falta o el exceso de cromosomas, es una característica presente en casi todos los tipos de cáncer humano y promueve el desarrollo de tumores.
La regulación de la mitosis es particularmente importante para mantener la estabilidad cromosómica. Por ejemplo, las células tumorales aneuploides aparecen como consecuencia de defectos en la segregación de cromosomas, los cuales originan células con mayor o menor material genético del normal.
Sin embargo, a pesar de su importancia, se conoce muy poco de la regulación de la salida de mitosis. En el artículo publicado en la revista Journal of Cell Science, el grupo de investigación de Ciclo Celular del IDIBELL, coordinado por Ethel Queralt, descubre un nuevo mecanismo de regulación de la salida de mitosis.
La proteína separasa es un componente clave para la correcta segregación de los cromosomas y para la regulación de la mitosis. En trabajos previos, el grupo de la doctora Queralt describió por primera vez la participación de la proteína Zds1 en la mitosis. Esta proteína coopera con la separasa para asegurar la correcta herencia genética de unas células a otras.
En el estudio, se profundiza en el mecanismo molecular por el cual esta proteína Zds1 regula la mitosis y contribuye a que la segregación de los cromosomas sea la correcta. En este trabajo se ha utilizado la levadura Saccharomyces cerevisiae (levadura de cerveza) como organismo modelo.
La levadura es uno de los organismos modelo más utilizado para estudiar los procesos básicos en la célula, que ha permitido identificar mecanismos moleculares complejos como el estudio del ciclo celular en organismos superiores. La aplicación de dichos conocimientos básicos ayudará a desarrollar tratamientos más específicos y directos contra los diferentes tipos de cáncer.
La doctora Queralt destaca que “los mecanismos de regulación de la mitosis son muy complejos y el hecho de conocerlos bien abre la puerta a fármacos específicos que permitan inhibir o corregir este proceso en diversas enfermedades, especialmente el cáncer”.
La investigadora explica que la mayoría de fármacos anticancerígenos se empiezan a aplicar sin conocer de manera exacta cómo actúan: “se trata de compuestos que muchas veces no sabemos cómo funcionan, pero lo hacen. Si seguimos un proceso inverso, es decir, si empezamos por conocer bien la actividad de una determinada proteína o de una parte de la proteína, podremos diseñar fármacos específicos minimizando los efectos secundarios”.
La investigación realizada por la Dra. Queralt es un paso importante para poder elaborar terapias que impidan que las células tumorales se repliquen.
La transmisión de la información genética (ADN) de padres a hijos (o lo que es equivalente, de unas células a otras) es una cuestión fundamental en la biología. La aneuploidia, es decir la falta o el exceso de cromosomas, es una característica presente en casi todos los tipos de cáncer humano y promueve el desarrollo de tumores.
La regulación de la mitosis es particularmente importante para mantener la estabilidad cromosómica. Por ejemplo, las células tumorales aneuploides aparecen como consecuencia de defectos en la segregación de cromosomas, los cuales originan células con mayor o menor material genético del normal.
Sin embargo, a pesar de su importancia, se conoce muy poco de la regulación de la salida de mitosis. En el artículo publicado en la revista Journal of Cell Science, el grupo de investigación de Ciclo Celular del IDIBELL, coordinado por Ethel Queralt, descubre un nuevo mecanismo de regulación de la salida de mitosis.
La proteína separasa es un componente clave para la correcta segregación de los cromosomas y para la regulación de la mitosis. En trabajos previos, el grupo de la doctora Queralt describió por primera vez la participación de la proteína Zds1 en la mitosis. Esta proteína coopera con la separasa para asegurar la correcta herencia genética de unas células a otras.
En el estudio, se profundiza en el mecanismo molecular por el cual esta proteína Zds1 regula la mitosis y contribuye a que la segregación de los cromosomas sea la correcta. En este trabajo se ha utilizado la levadura Saccharomyces cerevisiae (levadura de cerveza) como organismo modelo.
La levadura es uno de los organismos modelo más utilizado para estudiar los procesos básicos en la célula, que ha permitido identificar mecanismos moleculares complejos como el estudio del ciclo celular en organismos superiores. La aplicación de dichos conocimientos básicos ayudará a desarrollar tratamientos más específicos y directos contra los diferentes tipos de cáncer.
La doctora Queralt destaca que “los mecanismos de regulación de la mitosis son muy complejos y el hecho de conocerlos bien abre la puerta a fármacos específicos que permitan inhibir o corregir este proceso en diversas enfermedades, especialmente el cáncer”.
La investigadora explica que la mayoría de fármacos anticancerígenos se empiezan a aplicar sin conocer de manera exacta cómo actúan: “se trata de compuestos que muchas veces no sabemos cómo funcionan, pero lo hacen. Si seguimos un proceso inverso, es decir, si empezamos por conocer bien la actividad de una determinada proteína o de una parte de la proteína, podremos diseñar fármacos específicos minimizando los efectos secundarios”.
La investigación realizada por la Dra. Queralt es un paso importante para poder elaborar terapias que impidan que las células tumorales se repliquen.
Referencia
Baro B, Rodriguez-Rodriguez JA, Russiñol N, Queralt E, Calabria I. Zds1 regulates PP2ACdc55 activity and Cdc14 activation during mitotic exit via its Zds_C motif.. Journal of Cell Science. 2012 PMID: 22427694 [Epub ahead of print].
Baro B, Rodriguez-Rodriguez JA, Russiñol N, Queralt E, Calabria I. Zds1 regulates PP2ACdc55 activity and Cdc14 activation during mitotic exit via its Zds_C motif.. Journal of Cell Science. 2012 PMID: 22427694 [Epub ahead of print].

 Tendencias Científicas
Tendencias Científicas

 El corazón débil también daña al cerebro
El corazón débil también daña al cerebro CIENCIA ON LINE
CIENCIA ON LINE