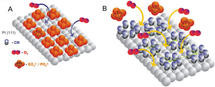
Ruptura del enlace de oxigeno. CSIC
Las pilas o células de combustible convierten la energía química en eléctrica utilizando como reactivos habituales el hidrógeno en el ánodo y el oxígeno en el cátodo. Las placas del electrodo suelen estar cubiertas por un catalizador, como el platino. Que sean más o menos potentes depende del producto del voltaje de la pila por la corriente eléctrica que fluye cuando se cierra el circuito. Esta corriente es equivalente a la velocidad de dos reacciones electroquímicas: la oxidación del hidrógeno y la reducción del oxígeno.
Ahora, un equipo internacional de investigadores ha logrado multiplicar por 10 la velocidad a la que transcurre la reducción de oxígeno sobre platino, una reacción electroquímica de la que depende la potencia eléctrica proporcionada por las pilas de combustible. El nuevo método podría permitir fabricar cátodos para estas pilas con una cantidad mucho menor de platino, lo que las haría económicamente más competitivas.
El estudio, que se publica en el último número de la revista Nature Chemistry, lo han desarrollado investigadores del Instituto de Química Física ‘Rocasolano’, (CSIC), del Argonne National Laboratory (Illinois, EEUU) y de un laboratorio de I+D de una compañía japonesa fabricante de coches.
“Una de las principales limitaciones para el desarrollo de este tipo de tecnología es la baja velocidad a la que ocurre la reducción de oxígeno, lo que implica menor potencia para un mismo voltaje”, explica Ángel Cuesta, coautor del trabajo e investigador del CSIC. “Y además, que haya que utilizar grandes cantidades de platino para conseguir la potencia deseada encarece demasiado las pilas de combustible”.
El equipo ha centrado su atención en manipular los átomos presentes en la superficie del platino, un metal normalmente empleado como catalizador de la pila por ser el más activo en acelerar la reacción química necesaria para generar electricidad.
“Hemos intentado mantener las propiedades químicas de los átomos superficiales del platino y hemos modificado el tamaño y la estructura geométrica de los grupos de átomos de platino expuestos al medio interno de la pila o electrolito”, explica el científico.
Durante los experimentos, los investigadores consiguieron retener moléculas de cianuro sobre la superficie de un electrodo de platino con el objetivo de que quedasen dos o tres átomos de platino en línea, necesarios para que se rompiese el enlace O-O en la molécula de oxígeno (O2).
“De esta forma, la velocidad a la que transcurre la reducción de oxígeno se multiplica por 10 empleando ácido fosfórico como conductor eléctrico y por 25 en el caso de ácido sulfúrico”, destaca Cuesta.
Ahora, un equipo internacional de investigadores ha logrado multiplicar por 10 la velocidad a la que transcurre la reducción de oxígeno sobre platino, una reacción electroquímica de la que depende la potencia eléctrica proporcionada por las pilas de combustible. El nuevo método podría permitir fabricar cátodos para estas pilas con una cantidad mucho menor de platino, lo que las haría económicamente más competitivas.
El estudio, que se publica en el último número de la revista Nature Chemistry, lo han desarrollado investigadores del Instituto de Química Física ‘Rocasolano’, (CSIC), del Argonne National Laboratory (Illinois, EEUU) y de un laboratorio de I+D de una compañía japonesa fabricante de coches.
“Una de las principales limitaciones para el desarrollo de este tipo de tecnología es la baja velocidad a la que ocurre la reducción de oxígeno, lo que implica menor potencia para un mismo voltaje”, explica Ángel Cuesta, coautor del trabajo e investigador del CSIC. “Y además, que haya que utilizar grandes cantidades de platino para conseguir la potencia deseada encarece demasiado las pilas de combustible”.
El equipo ha centrado su atención en manipular los átomos presentes en la superficie del platino, un metal normalmente empleado como catalizador de la pila por ser el más activo en acelerar la reacción química necesaria para generar electricidad.
“Hemos intentado mantener las propiedades químicas de los átomos superficiales del platino y hemos modificado el tamaño y la estructura geométrica de los grupos de átomos de platino expuestos al medio interno de la pila o electrolito”, explica el científico.
Durante los experimentos, los investigadores consiguieron retener moléculas de cianuro sobre la superficie de un electrodo de platino con el objetivo de que quedasen dos o tres átomos de platino en línea, necesarios para que se rompiese el enlace O-O en la molécula de oxígeno (O2).
“De esta forma, la velocidad a la que transcurre la reducción de oxígeno se multiplica por 10 empleando ácido fosfórico como conductor eléctrico y por 25 en el caso de ácido sulfúrico”, destaca Cuesta.

 Tendencias Científicas
Tendencias Científicas

 La Inteligencia Artificial puede ver a través del espejo
La Inteligencia Artificial puede ver a través del espejo CIENCIA ON LINE
CIENCIA ON LINE