
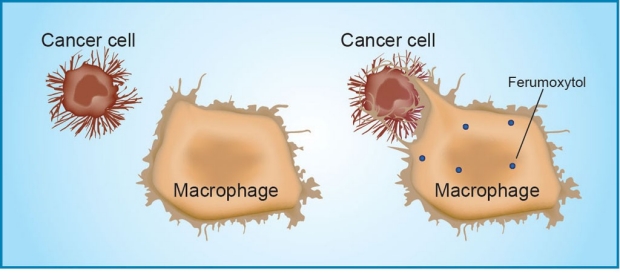
El ferumoxytol activa los macrófagos asociados con los tumores. Imagen: Amy Thomas. Fuente: Universidad Stanford.
Investigadores de la Universidad Stanford (California, EE.UU.) han descubierto accidentalmente que las nanopartículas de hierro inventadas para el tratamiento de la anemia tienen otro uso: activar la capacidad del sistema inmune para destruir las células tumorales.
Las nanopartículas, que están disponibles comercialmente en forma del suplemento de hierro inyectable ferumoxytol, están aprobadas por la Administración de Alimentos y Medicamentos estadounidense (FDA) para el tratamiento de la anemia por deficiencia de hierro.
Un estudio con ratones encontró que el ferumoxytol provoca que las células inmunes denominadas macrófagos asociados a tumores destruyan las células cancerosas. El descubrimiento, descrito en un artículo publicado en Internet en la revista Nature Nanotechnology, se hizo por accidente mientras se probaba si las nanopartículas podrían servir como caballos de Troya, introduciendo a escondidas quimioterapia en tumores de ratones.
"Fue muy sorprendente para nosotros que las nanopartículas activaran los macrófagos de manera que empezaron a atacar a las células cancerosas en los ratones", dice Heike Daldrup-Link, que es la autora principal del estudio y profesora ayudante de radiología en la Escuela de Medicina. "Creemos que este concepto debería mantenerse también en pacientes humanos."
El equipo de Daldrup-Link llevó a cabo un experimento con tres grupos de ratones: un grupo experimental que recibió nanopartículas cargadas con quimioterapia, un grupo de control que recibió nanopartículas sin quimio y un grupo de control que no recibió ni unas ni otras. Los investigadores hicieron la inesperada observación de que el crecimiento de los tumores en los animales que recibieron solamente nanopartículas desaparecía, en comparación con los otros grupos.
Macrófagos
Los investigadores llevaron a cabo una serie de pruebas de seguimiento para describir lo que estaba ocurriendo. Experimentando con células en un plato, demostraron que hacían falta unas células inmunes llamadas macrófagos asociados a tumores para que se produjera la actividad anti-cáncer de las nanopartículas; en cultivos de células sin macrófagos, las nanopartículas de hierro no tuvieron ningún efecto contra las células cancerosas.
Antes de este estudio, ya se sabía que en las personas sanas, los macrófagos asociados a tumores detectan y se comen las células tumorales individuales. Sin embargo, grandes tumores pueden secuestrar a estos macrófagos, haciendo que dejen de atacar y en su lugar comiencen a secretar sustancias que promueven el crecimiento del cáncer.
El estudio mostró que las nanopartículas de hierro devuelven a los macrófagos a su estado anti-cáncer, como demuestra el seguimiento de los productos del metabolismo de los macrófagos y el examen de sus patrones de expresión génica.
Además, en un modelo de ratón del cáncer de mama, los investigadores demostraron que el ferumoxytol inhibía el crecimiento del tumor cuando se administraba en dosis, ajustadas al peso corporal, similares a las aprobadas por la FDA para el tratamiento de la anemia.
Estudios anteriores habían demostrado que las nanopartículas se metabolizan durante un período de aproximadamente seis semanas, y el nuevo estudio muestra que el efecto anti-cáncer de una dosis única de nanopartículas disminuía en tres semanas aproximadamente.
Las nanopartículas, que están disponibles comercialmente en forma del suplemento de hierro inyectable ferumoxytol, están aprobadas por la Administración de Alimentos y Medicamentos estadounidense (FDA) para el tratamiento de la anemia por deficiencia de hierro.
Un estudio con ratones encontró que el ferumoxytol provoca que las células inmunes denominadas macrófagos asociados a tumores destruyan las células cancerosas. El descubrimiento, descrito en un artículo publicado en Internet en la revista Nature Nanotechnology, se hizo por accidente mientras se probaba si las nanopartículas podrían servir como caballos de Troya, introduciendo a escondidas quimioterapia en tumores de ratones.
"Fue muy sorprendente para nosotros que las nanopartículas activaran los macrófagos de manera que empezaron a atacar a las células cancerosas en los ratones", dice Heike Daldrup-Link, que es la autora principal del estudio y profesora ayudante de radiología en la Escuela de Medicina. "Creemos que este concepto debería mantenerse también en pacientes humanos."
El equipo de Daldrup-Link llevó a cabo un experimento con tres grupos de ratones: un grupo experimental que recibió nanopartículas cargadas con quimioterapia, un grupo de control que recibió nanopartículas sin quimio y un grupo de control que no recibió ni unas ni otras. Los investigadores hicieron la inesperada observación de que el crecimiento de los tumores en los animales que recibieron solamente nanopartículas desaparecía, en comparación con los otros grupos.
Macrófagos
Los investigadores llevaron a cabo una serie de pruebas de seguimiento para describir lo que estaba ocurriendo. Experimentando con células en un plato, demostraron que hacían falta unas células inmunes llamadas macrófagos asociados a tumores para que se produjera la actividad anti-cáncer de las nanopartículas; en cultivos de células sin macrófagos, las nanopartículas de hierro no tuvieron ningún efecto contra las células cancerosas.
Antes de este estudio, ya se sabía que en las personas sanas, los macrófagos asociados a tumores detectan y se comen las células tumorales individuales. Sin embargo, grandes tumores pueden secuestrar a estos macrófagos, haciendo que dejen de atacar y en su lugar comiencen a secretar sustancias que promueven el crecimiento del cáncer.
El estudio mostró que las nanopartículas de hierro devuelven a los macrófagos a su estado anti-cáncer, como demuestra el seguimiento de los productos del metabolismo de los macrófagos y el examen de sus patrones de expresión génica.
Además, en un modelo de ratón del cáncer de mama, los investigadores demostraron que el ferumoxytol inhibía el crecimiento del tumor cuando se administraba en dosis, ajustadas al peso corporal, similares a las aprobadas por la FDA para el tratamiento de la anemia.
Estudios anteriores habían demostrado que las nanopartículas se metabolizan durante un período de aproximadamente seis semanas, y el nuevo estudio muestra que el efecto anti-cáncer de una dosis única de nanopartículas disminuía en tres semanas aproximadamente.

Magnetita, u óxido de hierro (II, III), del que se obtienen las nanopartículas de hierro. Imagen: Archaeodontosaurus. Fuente: Pixabay.
Aplicaciones clínicas
Los científicos también probaron si las nanopartículas podrían detener la propagación del cáncer, o metástasis. En un modelo de ratón del cáncer de pulmón de células pequeñas, las nanopartículas redujeron la formación de tumores en el hígado, un sitio común de metástasis en ratones y seres humanos. En un modelo separado de la metástasis de hígado, un pretratamiento con nanopartículas antes de introducir células tumorales redujo en gran medida el volumen de los tumores del hígado.
Los resultados del estudio sugieren varias aplicaciones posibles para poner a prueba en ensayos humanos, dice Daldrup-Link en la nota de la universidad. Las nanopartículas de hierro carecen de los efectos secundarios tóxicos de la quimioterapia, lo que sugiere que se podrían dar a los pacientes durante el período de recuperación tras una cirugía por cáncer.
Con todo, el ferumoxytol también tiene efectos secundarios, entre ellos reacciones alérgicas graves o incluso mortales. Según la FDA, también puede producir problemas respiratorios, descenso de la presión sanguínea, mareos, inflamación, sarpullidos y picazón.
Las nanopartículas también pueden ayudar a los pacientes con cáncer cuyos tumores no pueden eliminarse por completo. "Si quedan algunas células tumorales después de una cirugía, pensamos que podría funcionar inyectar ahí nanopartículas de hierro" dice Daldrup-Link.
El hecho de que las nanopartículas ya estén aprobados por la FDA [para otros usos] acelera la capacidad de probar estas aplicaciones en seres humanos, agrega.
Los nuevos hallazgos también ayudarán a los investigadores del cáncer a realizar evaluaciones más precisas de los fármacos formados en parte por nanopartículas, dice Daldrup-Link. "En muchos estudios, los investigadores consideran solo las nanopartículas como vehículos para los fármacos", dice. "Pero podrían tener efectos intrínsecos ocultos que no vamos a apreciar a menos que nos fijamos en las propias nanopartículas."
Científicos de la Universidad de Ciencia y Salud de Oregón también contribuyeron al estudio.
Los científicos también probaron si las nanopartículas podrían detener la propagación del cáncer, o metástasis. En un modelo de ratón del cáncer de pulmón de células pequeñas, las nanopartículas redujeron la formación de tumores en el hígado, un sitio común de metástasis en ratones y seres humanos. En un modelo separado de la metástasis de hígado, un pretratamiento con nanopartículas antes de introducir células tumorales redujo en gran medida el volumen de los tumores del hígado.
Los resultados del estudio sugieren varias aplicaciones posibles para poner a prueba en ensayos humanos, dice Daldrup-Link en la nota de la universidad. Las nanopartículas de hierro carecen de los efectos secundarios tóxicos de la quimioterapia, lo que sugiere que se podrían dar a los pacientes durante el período de recuperación tras una cirugía por cáncer.
Con todo, el ferumoxytol también tiene efectos secundarios, entre ellos reacciones alérgicas graves o incluso mortales. Según la FDA, también puede producir problemas respiratorios, descenso de la presión sanguínea, mareos, inflamación, sarpullidos y picazón.
Las nanopartículas también pueden ayudar a los pacientes con cáncer cuyos tumores no pueden eliminarse por completo. "Si quedan algunas células tumorales después de una cirugía, pensamos que podría funcionar inyectar ahí nanopartículas de hierro" dice Daldrup-Link.
El hecho de que las nanopartículas ya estén aprobados por la FDA [para otros usos] acelera la capacidad de probar estas aplicaciones en seres humanos, agrega.
Los nuevos hallazgos también ayudarán a los investigadores del cáncer a realizar evaluaciones más precisas de los fármacos formados en parte por nanopartículas, dice Daldrup-Link. "En muchos estudios, los investigadores consideran solo las nanopartículas como vehículos para los fármacos", dice. "Pero podrían tener efectos intrínsecos ocultos que no vamos a apreciar a menos que nos fijamos en las propias nanopartículas."
Científicos de la Universidad de Ciencia y Salud de Oregón también contribuyeron al estudio.
Referencia bibliográfica:
Saeid Zanganeh, Gregor Hutter, Ryan Spitler, Olga Lenkov, Morteza Mahmoudi, Aubie Shaw, Jukka Sakari Pajarinen, Hossein Nejadnik, Stuart Goodman, Michael Moseley, Lisa Marie Coussens, Heike Elisabeth Daldrup-Link: Iron oxide nanoparticles inhibit tumour growth by inducing pro-inflammatory macrophage polarization in tumour tissues. Nature Nanotechnology (2016). DOI: 10.1038/nnano.2016.168.
Saeid Zanganeh, Gregor Hutter, Ryan Spitler, Olga Lenkov, Morteza Mahmoudi, Aubie Shaw, Jukka Sakari Pajarinen, Hossein Nejadnik, Stuart Goodman, Michael Moseley, Lisa Marie Coussens, Heike Elisabeth Daldrup-Link: Iron oxide nanoparticles inhibit tumour growth by inducing pro-inflammatory macrophage polarization in tumour tissues. Nature Nanotechnology (2016). DOI: 10.1038/nnano.2016.168.

 Tendencias Científicas
Tendencias Científicas

 El corazón débil también daña al cerebro
El corazón débil también daña al cerebro CIENCIA ON LINE
CIENCIA ON LINE