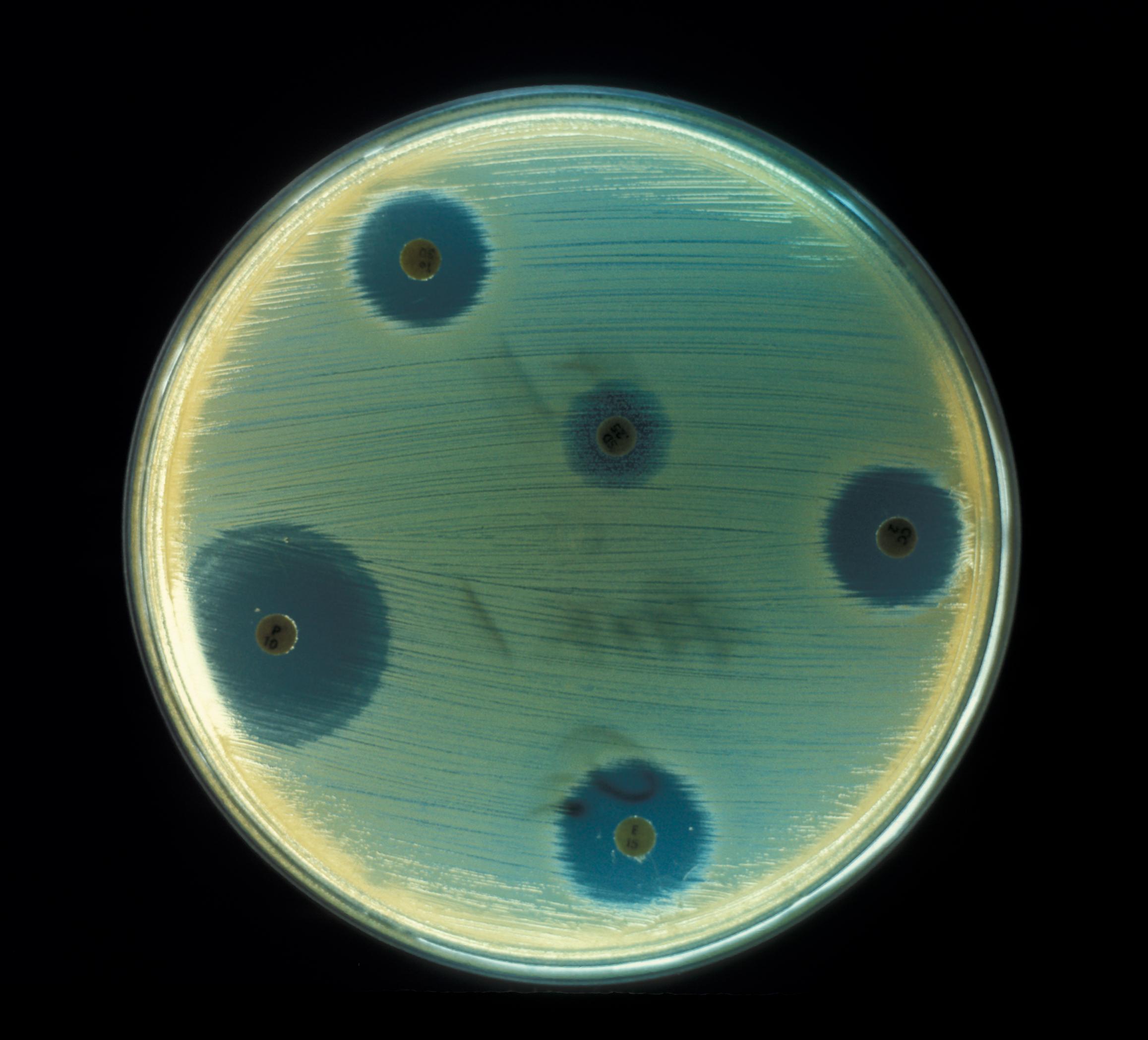
Test de susceptibilidad de la bacteria 'Staphylococcus aureus' a los antibióticos. Fuente: Centre for Disease Control/Wikipedia.
Investigadores de la Universidad Estatal de Oregón (Estados Unidos) han descubierto que los antibióticos tienen un impacto en los microorganismos que viven en el intestino de los animales más amplio y complejo de lo que se pensaba hasta ahora.
Los resultados ayudan a explicar mejor algunos de los daños que estos medicamentos pueden hacer, y sientan las bases para nuevas formas de estudiar y compensar dichos impactos. El trabajo ha sido publicado en línea en la revista Gut.
Los científicos saben desde hace tiempo que los antibióticos pueden tener efectos secundarios no deseados, especialmente la perturbación de la microbiota natural y beneficiosa del sistema gastrointestinal. Pero el nuevo estudio ayuda a explicar con más detalle por qué está sucediendo eso, y también sugiere que el uso de antibióticos potentes a largo plazo puede tener efectos aún más profundos.
Lo más problemático: el uso excesivo
Ahora se sospecha que el uso de antibióticos, y especialmente su uso excesivo, pueden tener efectos no deseados sobre el sistema inmune, el metabolismo de la glucosa, la absorción de alimentos, la obesidad, el estrés y el comportamiento.
Los problemas están aumentando en importancia, ya que el 40 por ciento de los adultos y el 70 por ciento de los niños toman uno o más antibióticos cada año, por no hablar de su uso en miles de millones de animales destinados al consumo.
Aunque cuando se utilizan correctamente los antibióticos pueden ayudar a tratar infecciones bacterianas potencialmente mortales, más del 10 por ciento de las personas que reciben estos medicamentos pueden sufrir efectos secundarios adversos.
"En la última década se ha abierto un universo completamente nuevo sobre los efectos de largo alcance del uso de antibióticos, y estamos explorándolo", explica en la nota de prensa de la universidad Andrey Morgun, profesor ayudante en la Facultad de Farmacia. "El estudio de la microbiota está justo explotando. Nada de lo que nos encontremos me sorprendería en este punto".
Los resultados ayudan a explicar mejor algunos de los daños que estos medicamentos pueden hacer, y sientan las bases para nuevas formas de estudiar y compensar dichos impactos. El trabajo ha sido publicado en línea en la revista Gut.
Los científicos saben desde hace tiempo que los antibióticos pueden tener efectos secundarios no deseados, especialmente la perturbación de la microbiota natural y beneficiosa del sistema gastrointestinal. Pero el nuevo estudio ayuda a explicar con más detalle por qué está sucediendo eso, y también sugiere que el uso de antibióticos potentes a largo plazo puede tener efectos aún más profundos.
Lo más problemático: el uso excesivo
Ahora se sospecha que el uso de antibióticos, y especialmente su uso excesivo, pueden tener efectos no deseados sobre el sistema inmune, el metabolismo de la glucosa, la absorción de alimentos, la obesidad, el estrés y el comportamiento.
Los problemas están aumentando en importancia, ya que el 40 por ciento de los adultos y el 70 por ciento de los niños toman uno o más antibióticos cada año, por no hablar de su uso en miles de millones de animales destinados al consumo.
Aunque cuando se utilizan correctamente los antibióticos pueden ayudar a tratar infecciones bacterianas potencialmente mortales, más del 10 por ciento de las personas que reciben estos medicamentos pueden sufrir efectos secundarios adversos.
"En la última década se ha abierto un universo completamente nuevo sobre los efectos de largo alcance del uso de antibióticos, y estamos explorándolo", explica en la nota de prensa de la universidad Andrey Morgun, profesor ayudante en la Facultad de Farmacia. "El estudio de la microbiota está justo explotando. Nada de lo que nos encontremos me sorprendería en este punto".
Estudio de cuatro antibióticos frecuentes
En la presente investigación se utilizó un "cóctel" de cuatro antibióticos frecuentemente suministrados a animales de laboratorio, para estudiar su impacto.
"Hasta ahora la mayoría de la gente pensaba que los antibióticos sólo agotaban la microbiota y disminuían varias funciones inmunes importantes que tienen lugar en el intestino", recuerda Morgun. "En realidad eso es sólo alrededor de un tercio del cuadro. También matan el epitelio intestinal, cuya destrucción es importante porque ahí es donde se absorben los nutrientes, forma parte de nuestro sistema inmunitario y tiene otras funciones biológicas en la salud humana".
La investigación también descubrió que los antibióticos y los microbios resistentes a los antibióticos causaban cambios significativos en la función mitocondrial, lo cual puede conducir a más muertes de células epiteliales.
Que los antibióticos tienen efectos especiales en las mitocondrias de las células es a la vez importante e interesante, añade Morgun, que co-lideró este estudio con Natalia Shulzhenko, investigadora de Medicina Veterinaria de la universidad.
La importancia de la mitocondria
La mitocondria juega un papel importante en la señalización celular, el crecimiento y la producción de energía, y deben funcionar correctamente para tener buena salud.
Pero la relación de los antibióticos con la mitocondria puede venir de muy atrás. En la evolución, las mitocondrias descienden de bacterias, que eran algunas de las primeras formas de vida, y diferentes bacterias competían entre sí por la supervivencia. Que un antibiótico todavía ataque selectivamente la porción de una célula que más se parece a las bacterias puede ser un recuerdo de ese arraigado sentido de la competencia y de la propia evolución de la vida.
El grupo de de Morgun y Schulzhenko también descubrió que uno de los genes afectados por el tratamiento con antibióticos es esencial para la comunicación entre los microbios y su huésped.
"Cuando el sistema de comunicación microbio-huésped se desequilibra puede producirse una cadena de problemas aparentemente sin relación", explica Morgun.
La disfunción digestiva está cerca de la parte superior de la lista, con problemas tales como la diarrea y la colitis ulcerosa. Pero una nueva investigación también está encontrando vínculos con la obesidad, la absorción de los alimentos, la depresión, la función inmune, sepsis, alergias y asma.
Bioinformática aplicada a la microbiótica
Esta investigación también ha desarrollado un nuevo enfoque de la bioinformática para estudiar la microbiota, que podría ayudar a acelerar aún más el estudio de las alteraciones de las interacciones de la microbiota huésped y la repercusión del antibiótico. Esto podría ayudar a la búsqueda de nuevos probióticos para ayudar a contrarrestar los efectos del antibiótico, y posiblemente conducir a sistemas que analicen el microbioma de una persona, identifiquen sus deficiencias y las aborden de una manera precisa e individual.
La microbiota saludable también puede ser otra manera de hacer frente a los problemas crecientes de la resistencia a los antibióticos, añde Morgun. En lugar de tratar de matar a las bacterias "malas" que causan una enfermedad, una microbiota saludable y funcional puede ser capaz de vencer a los microbios no deseados y mejorar la función inmune.
En la presente investigación se utilizó un "cóctel" de cuatro antibióticos frecuentemente suministrados a animales de laboratorio, para estudiar su impacto.
"Hasta ahora la mayoría de la gente pensaba que los antibióticos sólo agotaban la microbiota y disminuían varias funciones inmunes importantes que tienen lugar en el intestino", recuerda Morgun. "En realidad eso es sólo alrededor de un tercio del cuadro. También matan el epitelio intestinal, cuya destrucción es importante porque ahí es donde se absorben los nutrientes, forma parte de nuestro sistema inmunitario y tiene otras funciones biológicas en la salud humana".
La investigación también descubrió que los antibióticos y los microbios resistentes a los antibióticos causaban cambios significativos en la función mitocondrial, lo cual puede conducir a más muertes de células epiteliales.
Que los antibióticos tienen efectos especiales en las mitocondrias de las células es a la vez importante e interesante, añade Morgun, que co-lideró este estudio con Natalia Shulzhenko, investigadora de Medicina Veterinaria de la universidad.
La importancia de la mitocondria
La mitocondria juega un papel importante en la señalización celular, el crecimiento y la producción de energía, y deben funcionar correctamente para tener buena salud.
Pero la relación de los antibióticos con la mitocondria puede venir de muy atrás. En la evolución, las mitocondrias descienden de bacterias, que eran algunas de las primeras formas de vida, y diferentes bacterias competían entre sí por la supervivencia. Que un antibiótico todavía ataque selectivamente la porción de una célula que más se parece a las bacterias puede ser un recuerdo de ese arraigado sentido de la competencia y de la propia evolución de la vida.
El grupo de de Morgun y Schulzhenko también descubrió que uno de los genes afectados por el tratamiento con antibióticos es esencial para la comunicación entre los microbios y su huésped.
"Cuando el sistema de comunicación microbio-huésped se desequilibra puede producirse una cadena de problemas aparentemente sin relación", explica Morgun.
La disfunción digestiva está cerca de la parte superior de la lista, con problemas tales como la diarrea y la colitis ulcerosa. Pero una nueva investigación también está encontrando vínculos con la obesidad, la absorción de los alimentos, la depresión, la función inmune, sepsis, alergias y asma.
Bioinformática aplicada a la microbiótica
Esta investigación también ha desarrollado un nuevo enfoque de la bioinformática para estudiar la microbiota, que podría ayudar a acelerar aún más el estudio de las alteraciones de las interacciones de la microbiota huésped y la repercusión del antibiótico. Esto podría ayudar a la búsqueda de nuevos probióticos para ayudar a contrarrestar los efectos del antibiótico, y posiblemente conducir a sistemas que analicen el microbioma de una persona, identifiquen sus deficiencias y las aborden de una manera precisa e individual.
La microbiota saludable también puede ser otra manera de hacer frente a los problemas crecientes de la resistencia a los antibióticos, añde Morgun. En lugar de tratar de matar a las bacterias "malas" que causan una enfermedad, una microbiota saludable y funcional puede ser capaz de vencer a los microbios no deseados y mejorar la función inmune.
Referencia bibliográfica:
Andrey Morgun et al.: Uncovering effects of antibiotics on the host and microbiota using transkingdom gene networks. Gut (2015). DOI:10.1136/gutjnl-2014-308820.
Andrey Morgun et al.: Uncovering effects of antibiotics on the host and microbiota using transkingdom gene networks. Gut (2015). DOI:10.1136/gutjnl-2014-308820.